Onco-Digestif
Adénocarcinome de l’œsophage résécable : la chimiothérapie périopératoire par FLOT est un nouveau standard
La survie des patients ayant un adénocarcinome de l’œsophage résécable reste historiquement limitée. L’essai ESOPEC montre que, chez les patients en bon état général, une chimiothérapie périopératoire par FLOT améliore la survie globale à 3 ans comparativement à une chimioradiothérapie préopératoire.
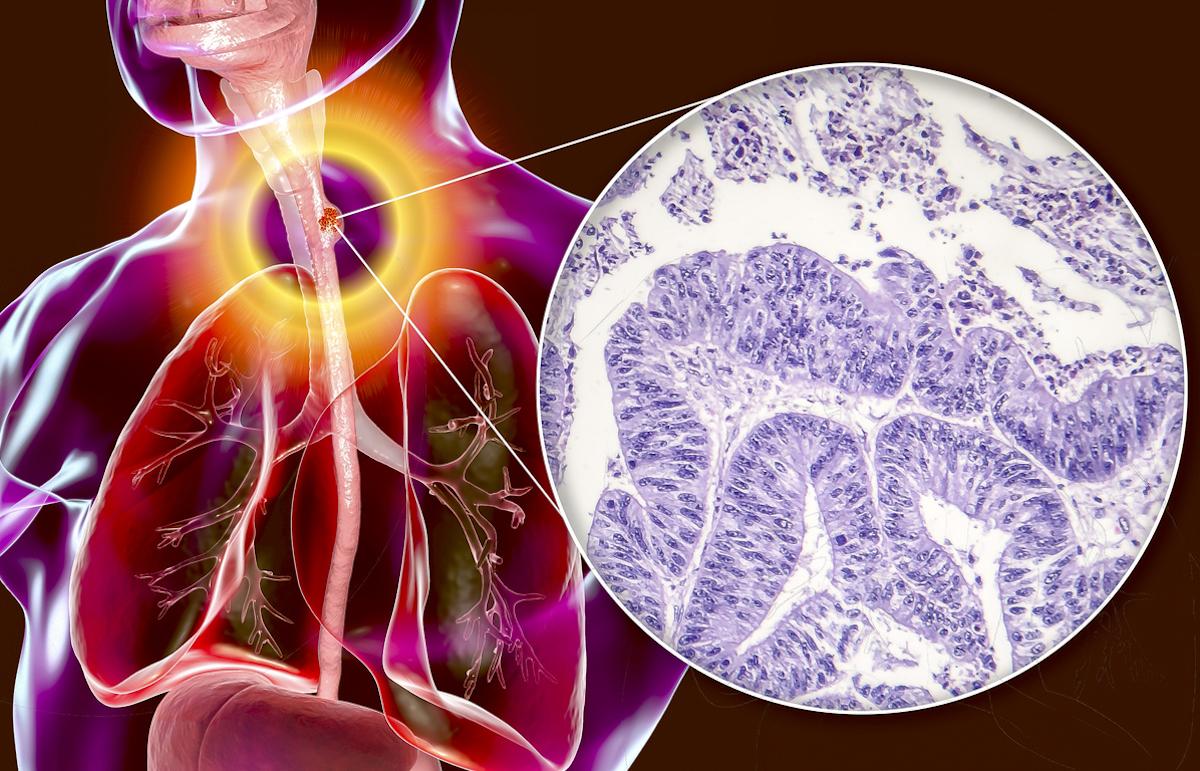
- Dr_Microbe/istock
Avec plus de 500 000 nouveaux cas annuels dans le monde, le cancer de l’œsophage figure parmi les tumeurs digestives les plus létales, causant plus de 445 000 décès chaque année. Si le carcinome épidermoïde domine dans la plupart des régions du globe, l’adénocarcinome de l’œsophage et de la jonction œsogastrique prédomine dans les pays occidentaux, où il représente jusqu’à 75 % des cancers œsophagiens. À l’heure actuelle, la prise en charge des formes non-métastatiques repose sur une stratégie multimodale associant chirurgie et traitement néoadjuvant ou périopératoire. Deux approches se sont, en effet, imposées récemment : la chimioradiothérapie préopératoire (carboplatine–paclitaxel + irradiation à 41,4 Gy), établie par l’étude CROSS et la chimiothérapie périopératoire, dont le protocole FLOT (fluorouracile, leucovorine, oxaliplatine, docétaxel) est devenu la référence après les essais FLOT4-AIO.
Dans l’essai ESOPEC, conduit chez 438 patients atteints d’adénocarcinome de l’œsophage résécable (cT1 N+ ou cT2–4a, sans métastase), on compare ces deux stratégies : FLOT (4 cycles avant et 4 cycles après la chirurgie) versus chimioradiothérapie préopératoire type CROSS suivie d’une chirurgie. Après un suivi médian de 55 mois, la survie globale à 3 ans atteint 57,4 % (IC 95 % : 50,1–64,0) dans le groupe FLOT contre 50,7 % (IC 95 % : 43,5–57,5) avec chimioradiothérapie, soit un hazard ratio (HR) de 0,70 (p = 0,01). La survie sans progression à 3 ans est également supérieure (51,6 % versus 35,0 % ; HR = 0,66), montrant un avantage net pour la chimiothérapie périopératoire. Les résultats sont publiés dans le New England Journal of Medicine.
Une réponse pathologique complète plus fréquente avec FLOT
Concernant la tolérance, les effets indésirables de grade ≥ 3 concernent 58 % des patients du bras FLOT (120/207) contre 50 % (98/196) dans le bras chimioradiothérapie préopératoire. Les événements indésirables graves surviennent chez respectivement 47,3 % et 41,8 % des patients, reflétant l’intensité du protocole FLOT. Malgré cela, la mortalité périopératoire (à 90 jours) n’est que de 3,1 % dans le groupe FLOT contre 5,6 % dans le groupe chimioradiothérapie, suggérant un rapport bénéfice-risque favorable à la chimiothérapie périopératoire.
Par ailleurs, les taux de résection R0 (marge saine) sont élevés et similaires dans les deux groupes (environ 95 %). On note que la radiothérapie préopératoire a peu diminué les récidives locorégionales (9 cas) par rapport à FLOT (17 cas), alors qu’il s’agit de son principal intérêt théorique, tandis que les métastases à distance sont moins nombreuses avec FLOT. Après l'intervention chirurgicale, une réponse pathologique complète (pas de cancer invasif résiduel dans la tumeur primaire réséquée et les ganglions lymphatiques) a été observée chez un pourcentage plus élevé de patients dans le groupe FLOT (16,7 %) que dans le groupe chimioradiothérapie préopératoire (10,1 %).
Un nouveau standard dans l’adénocarcinome de l’œsophage résécable
L’essai ESOPEC est un essai de phase III multicentrique et randomisé (1:1), mené de 2016 à 2020, incluant des patients porteurs d’un adénocarcinome de l’œsophage localement avancé mais résécable, sans métastases. Les investigateurs ont comparé deux standard déjà validés, en s’intéressant avant tout à la supériorité de FLOT sur la chimioradiothérapie préopératoire pour la survie globale. Bien que le suivi ait été suffisamment long (médiane de 55 mois) pour constater un avantage significatif, il reste possible que la sélection de patients aptes à recevoir FLOT (plus intensive) biaise en partie la généralisabilité des résultats.
Selon un éditorial associé, ces données positionnent la chimiothérapie périopératoire par FLOT comme nouveau standard dans l’adénocarcinome de l’œsophage résécable lorsque l’état général et l’absence de comorbidités majeures permettent de tolérer ce protocole. La place de la radiothérapie pourrait se restreindre aux patients moins éligibles à une chimiothérapie intensive ou à ceux présentant un risque accru d’extension locorégionale.
Les perspectives de recherche incluent l’intégration de la biologie moléculaire, notamment l’expression du récepteur HER2 ou la caractérisation de l’instabilité microsatellitaire, afin de proposer des traitements combinés plus ciblés (immunothérapie, anticorps anti-HER2...). Enfin, le monitorage par ADN tumoral circulant (ctDNA) pourrait permettre une adaptation thérapeutique individualisée, notamment pour optimiser la chimiothérapie postopératoire.
En conclusion, l’essai ESOPEC démontre la supériorité de FLOT en périopératoire sur la chimioradiothérapie préopératoire pour l’adénocarcinome de l’œsophage. Cet important changement de paradigme suggère que la radiothérapie pourrait s’effacer au profit d’une intensification systémique, ouvrant la voie à une personnalisation accrue des traitements associant chimiothérapie et agents ciblés.


-1698922310.jpg)
-1718791925.jpg)



























