Oncologie
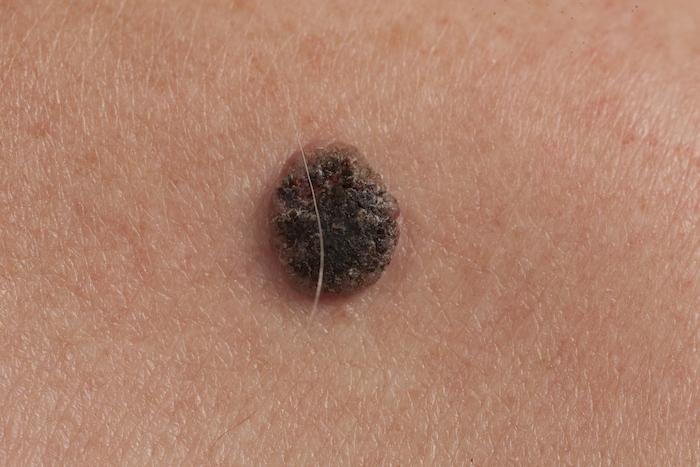
Mélanome stade 4 : association d’immunothérapies en adjuvant
Dans le traitement adjuvant du mélanome de stade 4 sans maladie apparente après résection, l’association ipilimumab-nivolumab fait beaucoup mieux que le nivolumab seul, mais au prix d’une toxicité très supérieure et qu’il convient désormais de réduire.
- Christoph Burgstedt/istock
L’immunothérapie par le nivolumab, un anti-PD1, est validée dans le traitement adjuvant du mélanome réséqué de stade III et IV à haut risque sur la fois d’une amélioration de la survie sans récidive dans une étude de phase III.
Dans une nouvelle étude multicentrique randomisée sur des mélanomes de stade IV sans maladie résiduelle après résection, l’association ipilimumab-nivolumab en adjuvant apparaît très supérieure par rapport au placebo, mais également par rapport au nivolumab seul (HR = 0,40 ; IC95 % 0,22-0,73), sur le pourcentage de récidive sans progression à 2 ans. Par contre, la toxicité de cette association à pleine dose est très élevée. L’étude a été présentée au congrès de l’ESMO 2019 à Barcelone.
Un bénéfice majeur de l’association
Après un suivi médian de 28,4 mois, la survie sans récidive est significativement plus longue pour le nivolumab que pour le placebo (RR = 0,56, IC à 95 % 0,36 à 0,88), et pour l’association nivolumab-ipilimumab par rapport au placebo (RR = 0,23, IC95 % 0,13 à 0,41). Ces résultats sont également cohérents dans l’analyse des sous-groupes pré-spécifiés.
Des effets indésirables de grade 3/4 liés au traitement ont été signalés dans 27% des cas du groupe nivolumab et dans 71% du groupe nivolumab-ipilimumab. Ces effets indésirables liés au traitement ont entraîné l'arrêt du traitement dans 13%, 62% et 2% des groupes nivolumab, nivo-ipi et placebo respectivement. Aucun décès lié au traitement n'a été signalé.
Une étude versus placebo
IMMUNED est une étude multicentrique de phase III, en double aveugle, sur 167 malades pour déterminer si le traitement adjuvant des mélanomes de stade IV sans maladie résiduelle après résection doit être basé sur le nivolumab seul (+ placebo) ou une association nivolumab (anti-PD1) et ipilimumab (anti-CTLA4).
Ils ont été randomisés entre 3 bras de traitement : soit nivolumab 3 mg/kg toutes les 2 semaines (n = 59) ou nivolumab 1 mg/kg plus ipilimumab 3 mg/kg toute les 3 semaines pour 4 doses, suivies de NIVO 3 mg/kg toutes les 2 semaines (n = 56), ou placebo (n = 52) pour une période pouvant atteindre 1 an (ou jusqu’à apparition d’une récidive, d’une toxicité inacceptable ou le retrait du consentement par le malade).
Des questions quant à la stratégie
Parmi les patients atteints de mélanome de stade IV sans maladie évidente après résection qui ont reçu un traitement adjuvant par nivolumab seul ou en association avec l’ipilimumab, il existe une augmentation significative de la survie sans récidive par rapport au placebo à 1 an comme à 2 ans.
Cette amélioration est particulièrement importante pour l’association anti-PD1/anti-CTLA4, mais cette augmentation de la survie sans récidive se fait au détriment de la tolérance avec des pourcentages d’effets indésirables de grade 3/4 particulièrement élevés dans le groupe association ipi-nivo, au-delà même des pourcentages observés chez les patients avec mélanome non-résécable de l’étude CheckMate 067.
Ces résultats traduisent donc l’intérêt des anti-CTLA4 dans le contrôle sur le long terme du mélanome et le bénéfice remarquable de l’association d’un inhibiteur de PD1 avec un immunostimulant anti-CTLA4. Ce bénéfice apparaît néanmoins au prix d’une toxicité qui amène à rechercher des stratégies de réduction de la toxicité de cette association tout en préservant son efficacité, soit en réduisant la durée de traitement, soit en réduisant les doses d’ipilimumab, par exemple à 1 mk/kg, soit en espaçant l’administration de l’ipilimumab, par exemple toutes les 6 semaines, d’après les auteurs.