Onco-Sein
Cancer du sein : de l’intérêt du curage axillaire
L’essai SENOMAC, confirme l’absence d’impact pronostique de l’abstention d’un curage axillaire chez des patients présentant un cancer du sein localisé, cN0 avec envahissement des ganglions sentinelles.
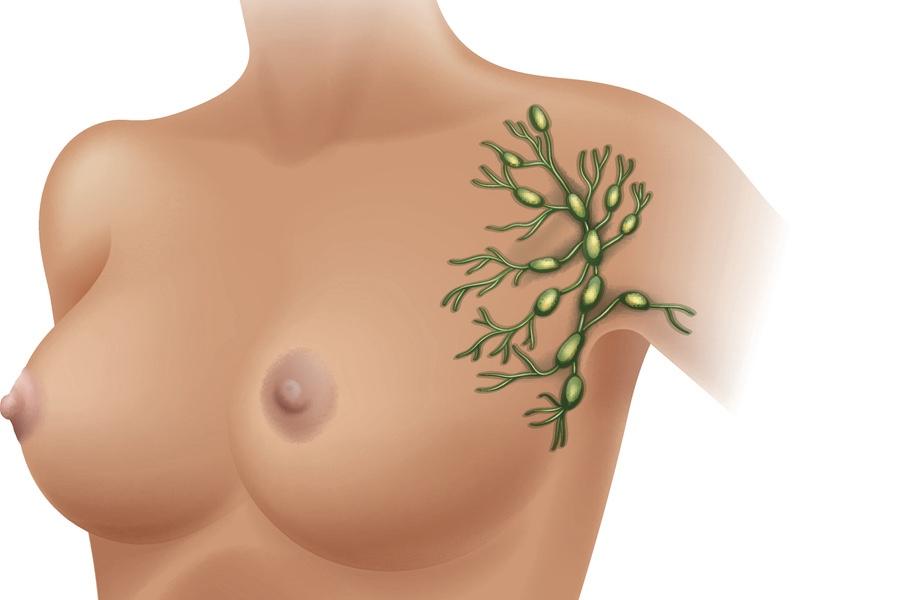
- blueringmedia/iStock
Deux principaux essais, Z0011 de l’ACOSOG et AMOROS de l’EORTC, ont démontré l’absence de bénéfice du curage axillaire extensif chez des patientes présentant un cancer du sein localisé, sans atteinte ganglionnaire clinique (cN0), mais avec envahissement d'un à 2 ganglions sentinelles, avec une réduction significative du risque de lymphœdème.
Ces essais avaient néanmoins plusieurs limites : tout d’abord un défaut de puissance nécessaire à la validation de leurs objectifs principaux et aussi un défaut de représentation de certains sous-groupes - comme les patients ayant bénéficié d'une mastectomie (exclus de l’essai ACOSOG Z0011 – 17,4 % des patients de l'essai AMOROS). Par ailleurs, les volumes cibles ganglionnaires utilisés, lors de la radiothérapie, dans l'essai ACOSOG Z0011 restent incertains. Ceci rendant plus difficile l’application en pratique clinique courante.
Ainsi, l’essai SENOMAC a pour objectif de valider ces résultats dans une large cohorte, en s’intéressant particulièrement aux sous-groupes faiblement représentés dans les précédentes études (mastectomie – extension extra-capsulaire – T3 – hommes).
Une population aux critères d’inclusion larges
Cet essai de phase III, de non-infériorité, a inclus 2 540 patientes atteints d'un cancer du sein localisé T1 à T3, cN0, avec envahissement macro métastatique d'un à 2 des ganglions sentinelles (effraction capsulaire et micrométastases supplémentaires autorisées). Les patientes étaient randomisées dans un bras curage axillaire (1 205 patientes) ou dans un bras sans curage (1 335 patientes). Les patientes dont les ganglions étaient non palpables cliniquement mais suspects en échographie étaient éligibles, même si la cytoponction ganglionnaire revenait positive.
L'âge médian des patientes était de 61 ans. Plus de 80 % des tumeurs étaient RE+ HER2-. Peu de tumeurs T3 (5,5 % et 6,1 % des tumeurs dans chacun des bras). L’atteinte ganglionnaire macro métastatique était majoritairement unique (85,6 % et 83,7 % dans chacun des bras), avec, pour un tiers, la présence d’une effraction capsulaire. Le nombre de patientes ayant bénéficiée d'une mastectomie était largement représentée (36 % des patientes). La majorité des patientes a bénéficié d'une radiothérapie incluant les volumes cibles ganglionnaires (89,9 % dans le bras sans curage et 88,4 % dans le bras avec curage).
A noter que 34,5 % des patientes ayant bénéficié d’un curage présentaient un envahissement ganglionnaire supplémentaire.
L’absence de curage non-inférieur à la réalisation d’un curage
Après un suivi médian de 46,8 mois, la survie globale à 5 ans était de 92,9 % (IC95 % : 91 – 94,9) dans le bras sans curage et de 92 % (IC95 % 89,9 – 94,1) dans le bras avec curage. La survie sans récidive à 5 ans était également équivalente dans chacun des 2 groupes : 89,7 % (IC95% : 87,5 – 91,9) dans le bras sans curage et de 88,7 % (IC95% : 86,3 – 91,1) dans le bras avec curage, HR 0,89 (IC95 % : 0,66 – 1,19).
Ces résultats semblent applicables aux différents sous-groupes, tels les patientes mastectomisées, avec une tumeur cT3 ou avec 2 macro-métastases ganglionnaires.
Une meilleure définition de la population de l’absence de curage
Ces résultats confirment les résultats des essais ACOSOG Z0011 et AMOROS, avec l’absence d’impact pronostique à une abstention du curage axillaire, chez les patientes présentant un cancer du sein localisé cT2 à cT3, cN0 avec envahissement tumoral d’un à 2 ganglions sentinelles et recevant un traitement adjuvant systémique et par radiothérapie, conformément aux directives nationales.
D’autres essais (OTAOSOR et SINODAR-ONE) confirmaient également ces résultats mais pour des populations à plus faible risque, l’intérêt de l’essai SENOMAC a été d’inclure une population plus large permettant de valider l’absence de curage dans certains sous-groupes à risque : effraction capsulaire – tumeur cT3 – mastectomie.