Pneumologie
Asthme sévère atypique : en cas d’éosinophilie, évoquer une vascularite
Une granulomatose éosinophilique avec polyangéite, ou GEPA, est une vascularite rare qui suit la plupart du temps l’aggravation d’un asthme sévère éosinophilique de l’adulte. Le diagnostic en est important car le traitement est différent.

- Ljupco/istock
L’asthme est une maladie hétérogène fréquente qui évolue dans un petit pourcentage de cas vers une forme sévère, parfois avec corticodépendance. Différentes biothérapies spécifiques ont permis d’améliorer la prise en charge de ces formes sévères d’asthme à condition de bien phénotyper ces malades afin de leur appliquer un traitement personnalisé.
Un piège devant l'asthme sévère éosinophilique chez l’adulte est la granulomatose éosinophilique avec polyangéite (GEPA), anciennement connue sous le nom de « syndrome de Churg-Strauss ». La GEPA se manifeste typiquement par un asthme hyperéosinophilique qui s'aggrave, une atteinte articulaire associée à différents signes de vascularite cutanée et neurologique essentiellement, chez une personne de la cinquantaine. Les deux maladies peuvent provoquer des symptômes respiratoires similaires, notamment une toux, un essoufflement et une respiration sifflante, ce qui peut compliquer le diagnostic, mais l’éosinophilie est plus élevée dans la GEPA et peut s’accompagner de signes généraux et d’atteintes d’organes.
L'asthme hyperéosinophilique est caractéristique de cette maladie, et une immunité T2 éosinophilique sous-jacente prédispose à la fois à l'asthme sévère éosinophilique, à la polypose naso-sinusienne (PNS) et à la GEPA. Il s’agit d’une vascularite systémique rare qui affecte principalement les petits et moyens vaisseaux sanguins, caractérisée par des granulomes extravasculaires, une hyperéosinophilie sanguine et tissulaire qui représente une cible pertinente pour les biothérapies de type anti-IL5, la cytokine surexprimée en cas d’éosinophilie. Le traitement actuel repose cependant essentiellement sur les corticoïdes et les immunosuppresseurs.
L’asthme éosinophilique joue un rôle central
L'asthme joue un rôle central dans la GEPA et est présent sous la forme d’un asthme éosinophilique (immunité T2) dans plus de 90% des cas, souvent sous la forme d’un asthme tardif et sévère de l’adulte. L'asthme précède généralement les manifestations systémiques de la maladie de plusieurs années (11 ans) et peut être associé à une éosinophilie qui devient progressivement une « hyperéosinophilie » avec un taux d’éosinophiles supérieur ou égal à 1500/mm³. L’aggravation de l’asthme précèderait généralement la GEPA de 3 à 6 mois.
La polypose nasosinusienne (PNS) est également associée à la GEPA et est également le reflet d'une maladie immunologique sous-jacente avec une immunité T2 éosinophilique, qui prédispose à l'asthme sévère éosinophilique et à la GEPA. L'asthme touche 90% des personnes atteintes de GEPA et précède en moyenne de 9 ans le diagnostic.
Le diagnostic de la GEPA peut être évoqué chez un patient présentant un asthme rebelle, une hyperéosinophilie sanguine et des antécédents d'allergies ou de problèmes de sinus, mais il doit être confirmé par la biopsie d'un tissu ou d'un organe atteint.
Une vascularite systémique et éosinophilique
La GEPA évolue généralement en trois phases. Au cours de la première phase, le symptôme principal est un asthme, qui peut être parfois sévère. Il est souvent accompagné d'une toux, d'une gêne respiratoire et d'une inflammation permanente des sinus. Progressivement peuvent apparaître des signes généraux qui incluent la fièvre, la fatigue, une diminution de l'appétit (anorexie), un amaigrissement et une altération de l'état général. En dehors d’une éosinophilie sanguine, la prise de sang peut révéler une inflammation dans le sang, comme une élévation de la CRP. Des anticorps anti-polynucléaires neutrophiles, ou ANCA, de type MPO, peuvent également être retrouvés.
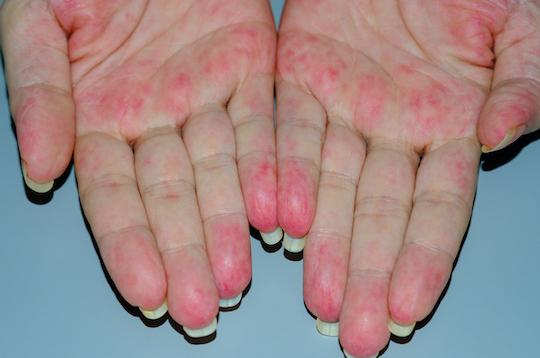
En l'absence de traitement, la GEPA peut toucher divers organes du corps, notamment les nerfs (3/4 des patients sous forme d’une mononévrite ou d’une multinévrite), le cœur (plus rarement sous la forme d’une myocardite ou d’une atteinte coronaire inflammatoire à l’origine d’infarctus), la peau (purpura ou nodules, qui ont l’avantage de pouvoir être facilement biopsiés et montrer une vascularite des vaisseaux de petit calibre et un infiltrat éosinophilique), le tube digestif (diarrhée et douleurs), les reins, les yeux, les muscles, les articulations et, plus rarement, le cerveau. Une hémorragie alvéolaire est une complication pulmonaire rare mais grave. La GEPA se distingue des autres vascularites par l'existence d'un asthme hyperéosinophilique.
Un traitement codifié en fonction du pronostic
Le traitement de la granulomatose éosinophilique avec polyangéite (GEPA) vise à réduire l'inflammation et à contrôler les symptômes. Il est organisé en fonction du pronostic de la maladie qui est établi en fonction d’un score, le Five Factor Score (FFS : protéinurie, créatininémie, cardiomyopathie spécifique, atteinte digestive grave et atteinte neurologique).
Les corticoïdes, tels que la prednisone, sont couramment utilisés pour réduire l'inflammation, éventuellement sous forme de bolus dans les formes graves. Ils sont indiqués seul en cas de FFS à 0 avec un sevrage progressif en cas de rémission. D'autres médicaments immunosuppresseurs, comme le cyclophosphamide, l’azthioprine, le rituximab et le méthotrexate, peuvent également être utilisés en association avec les corticoïdes en cas de FFS supérieur à 0, avec généralement un traitement d'attaque associant corticoïdes et cyclophosphamide, puis un sevrage des corticoïdes parallèlement à un traitement d’entretien en cas de rémission (azathioprine, MTX).
Le mépolizumab est un anticorps anti-interleukine-5 qui s'est avéré très efficace pour traiter l'asthme sévère éosinophilique et la PNS, et il est également indiqué dans le traitement des formes récidivantes ou réfractaires de la GEPA, à plus forte dose. La rémission est obtenue dans plus de 80% des patients avec ces protocoles. Si le traitement échoue ou si la réponse est insuffisante, des échanges plasmatiques peuvent être envisagés
En pratique, l'asthme sévère éosinophilique et la granulomatose éosinophilique avec polyangéite (GEPA) sont étroitement liés, car l'asthme T2 est un symptôme central et précurseur de la GEPA.
Références :
Cottin V et al. Respiratory manifestations of eosinophilic granulomatosis with polyangiitis (Churg-Strauss). Eur Respir J. 2016 Nov;48(5):1429-1441.
Groh M et al. Eosinophilic granulomatosis with polyangiitis (Churg-Strauss) (EGPA) Consensus Task Force recommendations for evaluation and management. Eur J Intern Med. 2015 Sep;26(7):545-53.