Hématologie
Myélome en rechute : ide-cel en vraie vie dans le registre français DESCAR-T
Cette étude issue du registre français DESCAR-T confirme l’efficacité et la faisabilité en vraie vie d’un traitement par le CAR-T cell idecabtagene vicleucel (ide-cel) pour le traitement du myélome multiple en rechute/réfractaire.
- Naeblys/istock
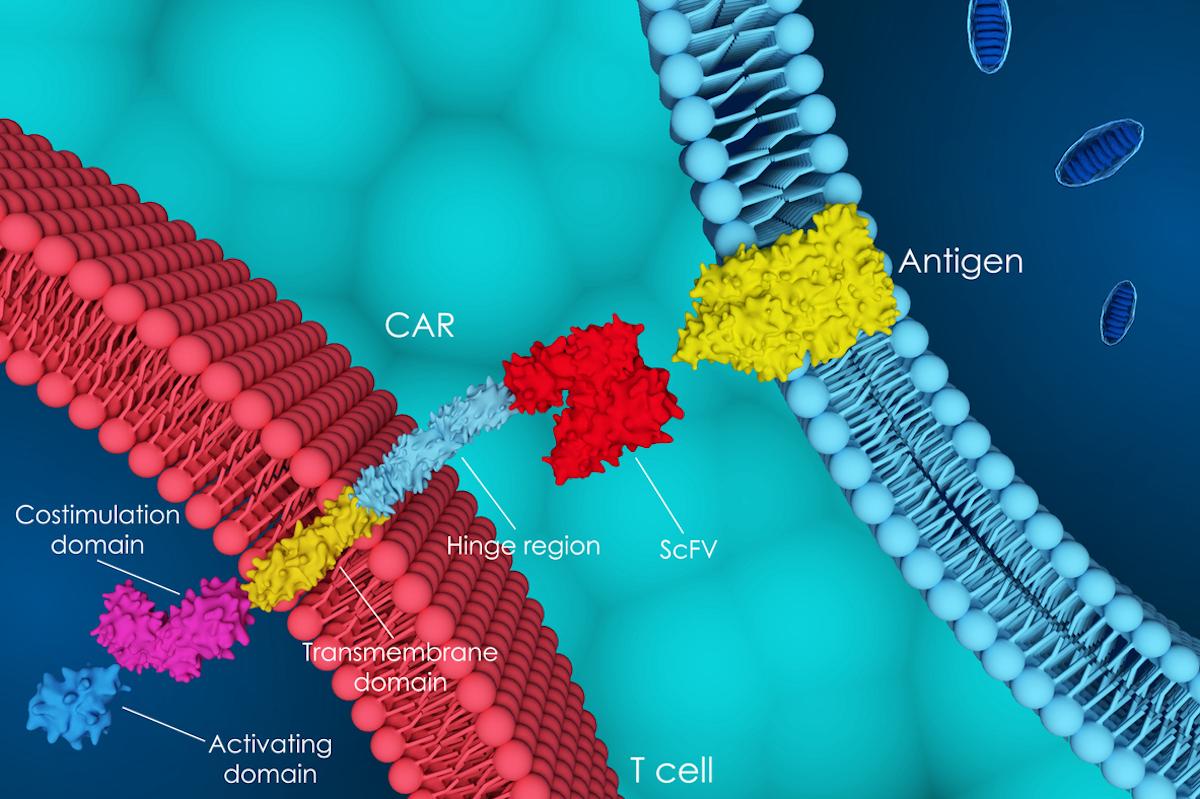
L’idecabtagene vicleucel (ide-cel), est un CAR-T cell anti-BCMA, disponible en France depuis avril 2021 pour le traitement du myélome multiple en rechute/réfractaire (MMRR).
Cette étude est issue du registre observationnel multicentrique DESCAR-T, auquel participent 11 hôpitaux français ayant accès au traitement par ide-cel.
Une population de myélomes multiples avancés
Dans ce registre, 176 patients atteints de MMRR ont bénéficié d’une aphérèse entre juin 2021 et novembre 2022. A noter, 58% (n=50) des patients n’auraient pas été incluables dans l’essai clinique KarMMa-3, principalement en raison de cytopénies, d’une insuffisance rénale ou des expositions thérapeutiques antérieures.
Parmi eux, 159 patients (90 %) ont effectivement reçu l’ide-cel ; 17 patients n’ont pas été réinjectés : 6 sont décédés, 3 car progression du myélome, 5 car échec de fabrication, 2 car refus et 1 sur décision du clinicien. L’âge moyen était de 61 ans (34-82), les patients avaient reçu en médiane 4 lignes de traitement (2-12), 79% étaient triple-réfractaires et 28% penta-réfractaires, 42% avaient un haut risque cytogénétique et 17% une maladie extra-médullaire (EMD).
Une toxicité limitée
Un syndrome de relargage cytokinique (SRC) est survenu chez 90 % des patients, dont 2 % seulement de grade ≥3, survenant en médiane dans les 24h après l’injection (0-16). Une neurotoxicité spécifique (ICANS) est survenue chez 12 % des patients, dont 3 % de grade ≥3, dans un délai médian de 1 jour (0-7) après l’injection.
Les cytopénies précoces -thrombopénie, neutropénie, anémie- était rapportées chez 35, 59 et 13% des patients, respectivement ; et les cytopénies tardives (à 6 mois) chez 11, 9 et 4% respectivement. Au cours des 6 premiers mois, 42% des patients ont présenté des infections de grade 3 ou plus.
Une maladie extra-médullaire ou une exposition antérieure aux anti-BCMA sont des facteurs de mauvais pronostic
Au cours des 6 premiers mois, les taux de meilleure réponse globale et de réponse complète étaient respectivement de 88 % et 47 %. La médiane de survie sans progression (SSP) à partir de l’injection d’ide-cel était de 12,5 mois, la survie globale (SG) médiane était de 20,8 mois et la SG estimée à 12 mois de 73,3 %.
Les patients avec une EMD avaient une SSP plus courte (6,2 mois contre 14,8 mois). En analyse multivariée, l’existence d’une EMD, d’une exposition antérieure à un traitement ciblant le BCMA, ou à un anticorps bi-spécifique anti-GPRC5D étaient associés à une SSP inférieure.
Conclusion
Au total, les résultats de SSP et de SG dans cette étude de registre sont similaires aux données rapportées dans les essais cliniques. La toxicité du traitement est limitée.
L’existence d’une EMD est péjorative, et les expositions thérapeutiques antérieures sont à prendre en compte pour optimiser la sélection des patients.