Hématologie
Waldenström en 1ère ligne : confirmation du schéma rituximab, cyclophosphamide et dexaméthasone (RCD)
La macroglobulinémie de Waldenström est un lymphome lymphoplasmocytaire rare, pour lequel il n’y a pas de consensus concernant le traitement de 1ère ligne. La combinaison rituximab, cyclophosphamide et dexaméthasone (RCD) permet de meilleurs taux de réponse et de survie globale en comparaison à un régime à base de bortézomib (VCD).
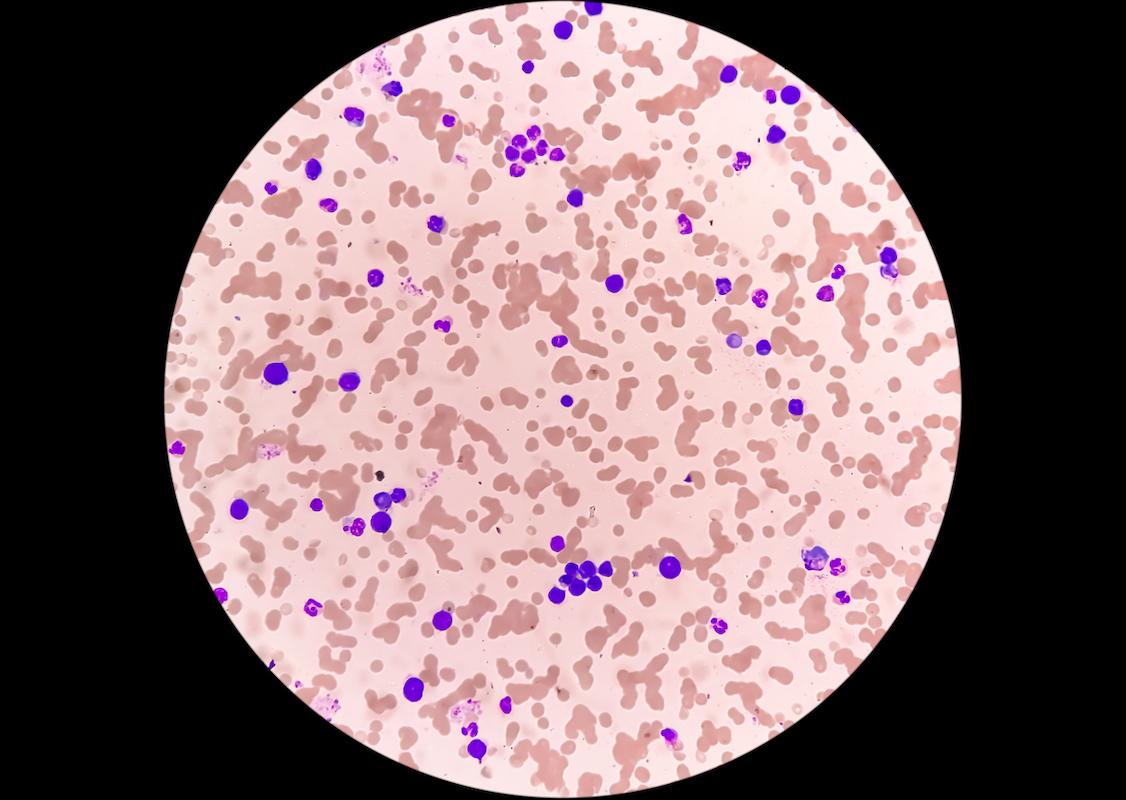
- Md Saiful Islam Khan/istock
La macroglobulinémie de Waldenström (MW) est un lymphome à cellules B rare caractérisé par la production d'une immunoglobuline M (IgM) monoclonale et l'infiltration de la moelle osseuse et d'autres organes par des des cellules lymphoplasmocytaires.
Cet essai randomisé contrôlé de phase III compare l'activité de la combinaison rituximab, cyclophosphamide et dexaméthasone (RCD) au bortézomib, cyclophosphamide et dexaméthasone (VCD) en 1ère ligne.
Caractéristiques de la population
Les patients recevaient six cycles de RCD (rituximab 375 mg/m² le jour 8 ; cyclophosphamide 500 mg/m² les jours 1, 8 et 15 ; et dexaméthasone 20 mg les jours 1, 2, 8, 9, 15, 16, 22 et 23) ou de VCD (bortézomib 1,6 mg/m² sous-cutané les jours 1, 8 et 15 du cycle de 28 jours ; cyclophosphamide 500 mg/m² les jours 1, 8 et 15 ; et dexaméthasone 20 mg les jours 1, 2, 8, 9, 15, 16, 22 et 23).
Au total, 40 patients ont été inclus. L'âge médian était de 62 ans (intervalle, 36-73). Quatre patients dans le groupe RCD et trois patients dans le groupe BCD avaient subi une plasmaphérèse.
Réponses plus durables avec le schéma RCD
Le taux de réponse global était le même dans les deux groupes (89,5% pour le groupe RCD vs. 89,5% avec le VCD ; P=1,000) ; réponse complète, n=1 (5,3%) vs 3 (15,8%) ; très bonne réponse partielle, n=7 (36,8%) vs 2 (10,5%) ; réponse partielle, n=9 dans chaque groupe. La durée médiane de la réponse dans le groupe RCD n'était pas atteinte vs 32,0 mois (intervalle de confiance [IC] à 95% : 15,6-48,4) dans le groupe VCD (RR = 0,2117, IC à 95% : 0,069-0,649 ; P=0,007).
Le suivi médian était de 55 mois (intervalle, 12-76). Cinq patients dans le groupe RCD et 13 dans le groupe VCD ont progressé. Le taux de survie sans progression (SSP) à 5 ans estimé dans le groupe RCD était de 69,4% (IC à 95% : 35%-88%), significativement plus élevé que le taux de 35,5% (IC à 95% : 15%-57%) dans le groupe VCD (P=0,009). La SSP médiane dans le groupe VCD était de 33,0 mois (IC à 95% : 15,7-50,3), plus courte que dans le groupe RCD (non atteint, ratio de risque [RR] = 0,324, IC à 95% : 0,121-0,774, P=0,009).
Un patient dans le groupe RCD et six dans le groupe VCD sont décédés. La survie globale médiane n'était pas atteinte et était de 70 mois dans les groupes RCD et BCD, respectivement.
Profil de tolérance similaire pour les 2 schémas
L'événement indésirable le plus courant de tout grade dans les deux groupes était la toxicité hématologique. Les grades des événements indésirables hématologiques et non hématologiques étaient similaires entre les deux groupes. Les événements indésirables non hématologiques courants dans le groupe RCD incluaient la fièvre non infectieuse (26,3%), la pneumonie (21,1%) et l'hyperglycémie (15,8%). Les événements indésirables non hématologiques courants dans le groupe VCD incluaient la neuropathie périphérique (26,3%), la pneumonie (21,2%), le zona (10,5%).
Le régime à base de rituximab, RCD, est supérieur ans cette étude au régime à base de bortézomib en termes de taux de survie sans progression et de survie globale. Le profil de tolérance du RCD en fait un choix sûr pour le traitement de première ligne de la MW.